ဒြပ်စင်အလှည့်ကျဇယား
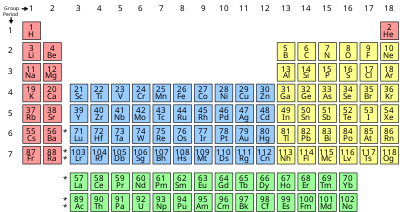
၁၈၆၉ တွင် ရုရှားဓာတုဗေဒပညာရှင် ဒမီသရီ အီဗန်နိုဗစ် မန်းဒယ်လိယပ် (Dmitri Evanovich Mendeleev) မှ ရာစုနစ် များစွာက တွေ့ရှိခဲ့ကြသည့် ဒြပ်စင်များအား ဓာတုဂုဏ်သတ္တိများပါဝင်သော ဒြပ်စင်အလှည့်မှန်ဇယား (periodic table) တစ်ခုအဖြစ် ရေးဆွဲထုတ်ဖော် ခဲ့သည်။ periodic table သည် သဘာဝ၏ ဥပဒေသများကို လိုက်နာကိုယ်စားပြုသည်။ အက်တမ်များ၏ အက်တမ်အမှတ်စဉ်ကို စီစဉ်ပေးခြင်းအားဖြင့် တိကျသော ၎င်းတို့၏ ဂုဏ်သတ္တိများကို သိသာထင်ရှားစွာ မြင်သာ စေသည်။ ထို့ကြောင့် ဓာတုဒြပ်စင်များ၏အကြောင်းကို အလွယ်တကူ သိရှိနိုင်သည်။
ဓာတု ဒြပ်စင်များ နှင့် ဒြပ်စင်အလှည့်မှန်ဇယား သမိုင်း
[ပြင်ဆင်ရန်]၁၆၆၉ ခုနစ်တွင် ဂျာမန် လူမျိုး သိပ္ပံပညာရှင် (German merchant and amateur alchemist Hennig Brand) သည် စိတ်ကူးယဉ်ဆန်သော Philosopher’s Stone အား ဖန်တီးရန် စတင်ကြိုးစားခဲ့သည်။ ၎င်းကျောက်တုံးသည် အရာဝထ္တုတစ်ခုကို သန့်စင်ကောင်းမွန်သော ရွှေအဖြစ်သို့ ပြောင်းလဲနိင်မည်ဟု တွေးထင်ခဲ့သည်။ Henning Brand သည် ပွက်ပွက်ဆူပြီးသော ဆီး( urine ) မှ အကြွင်းအကျန်များအား အပူပေးခဲ့သည်။ အရည်များ ကုန်ဆုံးသွားသည့်အခါ မီးတောက်ငယ်များအဖြစ် တောက်လောင် သွားကြသည်။ ၎င်းစမ်းသပ်မှုသည် ပထမဦးဆုံးသော ဖော့စဖော့ရပ်စ် (phosphorus) ရှာဖွေမှု ဖြစ်ခဲ့သည်။

၁၆၈၀ တွင် Robert Boyle သည်လည်း phosphorus ကို ရှာဖွေ တွေ ရှိခဲ့သည်။
၁၈၀၉ ခုနစ်တွင် ဒြပ်စင် ၄၇ မျိုးအထိ ရှာဖွေနိုင်ခဲ့ကြသည်။ သိပ္ပံပညာရှင်များသည် ၎င်းဒြပ်စင်များ၏ ဝိသေသ လက္ခဏာများအား သိရှိနိုင်စေရန် ဆက်လက် ကြိုးစားခဲ့ကြသည်။ ၁၈၆၃ ခုနစ်တွင် အင်္ဂလိပ် ဓာတုဗေဒပညာရှင် John Newlands သည် ရှာဖွေတွေရှိခဲ့သောဒြပ်စင် ၅၆ မျိုးအား အုပ်စု ၁၁ အုပ်စုအဖြစ် ဖွဲစည်းခဲ့သည်။
၁၈၆၉ ခုနစ်တွင် ရုရှား ဓာတုဗေဒပညာရှင် ဒမီသရီ အီဗန်နိုဗစ် မန်းဒယ်လိယပ် သည်ဒြပ်စင်များ၏ အက်တမ်အမှတ်စဉ်အရ အလှည့်မှန်ဇယားကို ရေးဆွဲခဲ့သည်။ သူသည် နောက်ထပ် တွေ့ရှိမည်ဖြစ်သော ဒြပ်စင်များအကြောင်းကိုပင် ကြိုတင်ပြောကြားခဲ့ပြီး ၎င်းဒြပ်စင်များအတွက် နေရာများအား ဇယားတွင် ချန်လှပ်ထားခဲ့သည်။
၁၈၈၆ ခုနစ်တွင် ပြင်သစ် ရူပဗေဒပညာရှင် (Antoine Bequerel) သည် ရေဒီယိုသတ္တိကြွစွမ်းအင်အား ပထမဆုံးရှာဖွေတွေ့ ရှိခဲ့သည်။ ထို့နောက် နယူးဇီလန် တက္ကသိုလ်မှ ကျောင်းသား သွန်ဆမ်သည် ရေဒီယိုသတ္တိကြွခြင်းမှ alpha, beta and gamma ဟုခေါ်သော ရောင်ခြည် ၃ မျိုးအား အမည်နာမ သတ်မှတ်ခဲ့သည်။
၁၈၉၄ ခုနစ်တွင် Sir William Ramsay နှင့် Lord Rayleigh တို့သည် အစွမ်းမဲ့ ဓာတ်ငွေ့များ (nobel gas) ကို ရှာဖွေတွေ့ရှိခဲ့ကြသည်။ ထိုဓာတ်ငွေ့များအား အလှည့်မှန်ဇယား၏ အုပ်စုနံပါတ် သုညတွင် ထည့်သွင်း သတ်မှတ်ခဲ့သည်။
၁၈၉၇ ခုနစ်တွင် အင်္ဂလိပ် ရုပဗေဒပညာရှင် ဂျေဂျေ သော်မဆင် (J. J. Thomson) သည် အက်တမ် တခုတွင် လျှပ်စစ်ဓာတ်မ စွမ်းအင်ရှိသော အီလက်ထရွန်များကို ရှာဖွေတွေ့ရှိခဲ့သည်။ John Townsend နှင့် Robert Millikan တို့သည် ၎င်းအီလက်ထရွန်များ၏ ထုထည် (mass) နှင့် တိကျသော လက္ခဏာ (exact charge) ကို အတိအကျရှာဖွေခဲ့ကြသည်။
၁၉၀ဝ တွင် Bequerel သည် အီလက်ထရွန် နှင့် ဘီတာအမှုန် (beta particles) များကို ဆက်လက် ရှာဖွေနိုင်ခဲ့သည်။ ၁၉၀၃ ခုနစ်တွင် Rutherford သည် အက်တမ်းများ ပျက်စီးယို့ယွင်းခြင်းအားဖြင့် ရေဒီယို သတ္တိကြွမှု ဖြစ်ပေါ်သည်ဟု ကြေညာခဲ့သည်။
၁၉၁၁ ခုနစ်တွင် Rutherford နင့် ဂျာမန် ရူပဗေဒပညာရှင် Hans Geiger တို့သည် အက်တမ်၏ နျူကလိယပ်စ်အား အီလက်ထရွန်များ လှည့်ပတ်နေသည်ဆိုသော အကြောင်းအရာအား ရှာဖွေခဲ့ကြသည်။
၁၉၁၃ ခုနစ် သိပ္ပံပညာရှင် Bohr ၏ တွေ့ရှိချက်အရ အီလက်ထရွန်များသည် နျူထရွန်များ၏ ဘေးပတ်လည်တွင် ခြားနားသော စွမ်းအင်များနှင့်အတူ ပတ်လမ်း (orbit ) ဟုခေါ်သော လမ်းကြောင်းဖြင့် လှည့်ပတ်နေကြသည်ကို သိရှိခဲ့ကြသည်။ အီလက်ထရွန်များ ပတ်လမ်းကြောင်းတစ်ခု မှ တစ်ခု ရွေ့ပြောင်းသောအခါတွင် ရေဒီယိုသတ္တိကြွခြင်း ဖြစ်ပေါ်လာခြင်း ဖြစ်သည်ကိုလည်း ဖော်ပြခဲ့သည်။
၁၉၁၄ ခုနစ်တွင် Rutherford သည် အက်တမ်၏ နျူကလီးယပ် ထဲတွင်ရှိသော ပရိုတွန်ကို အတိအကျ ရှာဖွေတွေရှိခဲ့သည်။
၁၉၃၂ တွင် James Chadwick သည် ပထမဆုံး နျူထရွန်ကို ရှာဖွေတွေ ့ရှိခဲ ့သည်။ isotopes များကိုလည်း ထပ်မံ တွေ့ရှိခဲ့သည်။ ၎င်းတိုသည် ဒြပ်စင်အလှည့်မှန်ဇယားအတွက် အခြေခံအား ပြီးပြည့်စုံစေသည်။ ၎င်းနှစ်တွင်ပင် Cockroft နှင့် the Irishman Walton တို့သည်လည်း အမှုန်တစ်ခုထဲရှိ အက်တမ်တစ်ခုအား အမှုန်အရှိန်မြှင့် ကိရိယာထဲတွင် လီသီယမ် နှင့် ရိုက်ခတ်လိုက်သောအခါ ဟီလီယမ် ၂ ခု အဖြစ်ပြောင်းလဲသွားသည် ကိုထပ် မံတွေ့ရှိခဲ့သည်။
၁၉၄၅ တွင် Glenn Seaborg သည် lanthanides နှင့် actinides (atomic number 92U ထက်များသော ဒြပ်စင်) များကို တွေ့ရှိခဲ့သည်။ ၎င်းတို့အား ဇယား၏အောက်ခြေတွင် တွေ့ရှိရသည်။[၁]
ရင်းမြစ်
[ပြင်ဆင်ရန်]- ↑ MUCTR-MM, ဘာသာပြန်သူ ကျော်ဇင်ထွဋ် [၁] Archived 13 February 2010 at the Wayback Machine.
အခြားကြည့်ရန်
[ပြင်ဆင်ရန်]| ဒြပ်စင်အလှည့်ကျဇယား | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
